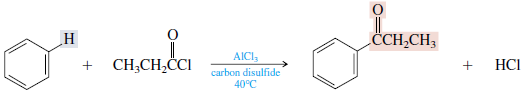
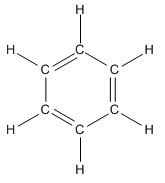
Benzena merupakan salah satu senyawa organik yang hanya terdiri dari enam atom karbon dan masing-masing atom karbon mengikat satu buah atom hidrogen. Atom hidrogen yang terikat pada atom karbon dapat tersubstitusi. Halaman ini akan menjelaskan substitusi atom hidrogen dalambenzena (senyawa turunan benzena dan manfaatnya).
Toluena digunakan untuk pelarut dalam industri, thinner cat, lem, tinta, resin, dsb.
Penggunaan anilina paling banyak adalah sebagai bahan baku pewarna diazo. Selain itu anilina dimanfaatkan untuk pembuatan poliuretan, dengan sebelumnya direaksikan terlebih dahulu dengan fosgen menjadi metilen difenil diisosianat. Penggunaan anilina yang lain adalah untuk membuat herbisida dan proses kimia dalam pembuatan penghapus karet.
Nitrobenzena digunakan untuk pengkilap lantai, pelarut cat, dan penyemir jaket kulit.
Asam benzoat dan garamnya digunakan untuk mengawetkan makanan, yang biasanya mempunyai kode E210, E211, E212, and E213. Kadar asam benzoat dalam makanan berkisar antara 0,05-0,1%. Asam benzoat terbukti mampu menghambat pertumbuhan bakteri dan jamur.
Asam benzoat juga digunakan sebagai larutan standar untuk mengtahui kapsitas kalor pada kalorimeter bom. Di bidang medis, asam benzoat digunakan untuk perawatan kulit akibat jamur.
Benzaldehida banyak digunakan untuk membuat perisa almond pada makanan maupun minuman. Penggunaan lain dari benzaldehida adalah untuk pestisida dan sebagai intermediet untuk mensintesis senyawa organik yang lain.
Penggunaan asam benzena sulfonat adalah untuk pembuatan obat (berupa garamnya).
Fenol banyak digunakan untuk pembuatan bisfenol-A dengan mereaksikannya dengan aseton. Selain itu, fenol juga berpotensi sebagai desinfektan. Dalam bidang farmasi, fenol banyak digunakan untuk membuat beberapa jenis obat, di antaranya obat faringitis.
Benzena Monosubstitusi
Benzena monosubstitusi adalah senyawa turunan benzena yang salah satu atom hidrogennya diganti dengan gugus fungsional yang lain. Ada banyak sekali benzena monosubstitusi, di antaranya:Toluena
Toluena adalah senyawa turunan benzena yang salah satu atom hidrogennya tersubstitusi oleh gugus metil (-CH3). Nama lain toluena adalah metil benzena. Dengan demikian toluena mempunyai rumus molekul C6H5CH3.Toluena digunakan untuk pelarut dalam industri, thinner cat, lem, tinta, resin, dsb.
Anilina
Anilina adalah senyawa turunan benzena yang salah satu atom hidrogennya tersubstitusi oleh gugus amina (-NH2). Dengan demikian anilina mempunyai rumus molekul C6H5NH2.Penggunaan anilina paling banyak adalah sebagai bahan baku pewarna diazo. Selain itu anilina dimanfaatkan untuk pembuatan poliuretan, dengan sebelumnya direaksikan terlebih dahulu dengan fosgen menjadi metilen difenil diisosianat. Penggunaan anilina yang lain adalah untuk membuat herbisida dan proses kimia dalam pembuatan penghapus karet.
Nitrobenzena
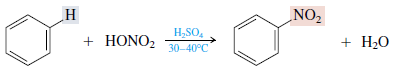
Nitrobenzena adalah senyawa turunan benzena yang salah satu atom hidrogennya tersubstitusi oleh gugus nitro (-NO2). Dengan demikian nitrobenzena mempunyai rumus molekul C6H5NO2.Nitrobenzena digunakan untuk pengkilap lantai, pelarut cat, dan penyemir jaket kulit.
Asam benzoat
Asam benzoat adalah senyawa turunan benzena yang salah satu atom hidrogennya tersubstitusi oleh gugus asam karboksilat (-COOH). Dengan demikian asam benzoat mempunyai rumus molekul C6H5COOH.Asam benzoat dan garamnya digunakan untuk mengawetkan makanan, yang biasanya mempunyai kode E210, E211, E212, and E213. Kadar asam benzoat dalam makanan berkisar antara 0,05-0,1%. Asam benzoat terbukti mampu menghambat pertumbuhan bakteri dan jamur.
Asam benzoat juga digunakan sebagai larutan standar untuk mengtahui kapsitas kalor pada kalorimeter bom. Di bidang medis, asam benzoat digunakan untuk perawatan kulit akibat jamur.
Benzaldehida
Benzaldehida adalah senyawa turunan benzena yang salah satu atom hidrogennya tersubstitusi oleh gugus aldehida (-CHO). Dengan demikian benzaldehida mempunyai rumus molekul C6H5COOH.Benzaldehida banyak digunakan untuk membuat perisa almond pada makanan maupun minuman. Penggunaan lain dari benzaldehida adalah untuk pestisida dan sebagai intermediet untuk mensintesis senyawa organik yang lain.
Asam benzena sulfonat
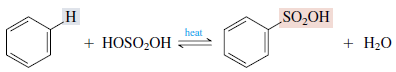
Asam benzena sulfonat adalah senyawa turunan benzena yang salah satu atom hidrogennya tersubstitusi oleh gugus asam sulfonat (-SO3H). Dengan demikian benzaldehida mempunyai rumus molekul C6H5SO3H.Penggunaan asam benzena sulfonat adalah untuk pembuatan obat (berupa garamnya).
Fenol
Fenol adalah senyawa turunan benzena yang salah satu atom hidrogennya tersubstitusi oleh gugus hidroksi (-OH). Dengan demikian fenol mempunyai rumus molekul C6H5OH. Walaupun mempunyai gugus fungsi alkohol, sifat fenol berbeda dengan alkohol. Fenol mempunyai gugus hidroksi yang terikat pada karbon tak jenuh. Fenol mempunyai keasaman yang tinggi karena cincin aromatik yang bergandengan kuat dengan oksigen dan cenderung memutuskan ikatan antara oksigen dan hidrogen.Fenol banyak digunakan untuk pembuatan bisfenol-A dengan mereaksikannya dengan aseton. Selain itu, fenol juga berpotensi sebagai desinfektan. Dalam bidang farmasi, fenol banyak digunakan untuk membuat beberapa jenis obat, di antaranya obat faringitis.