Pengertian Ikatan Kovalen
Ikatan kovalen adalah ikatan kimia yang terjadi jika adanya penggunaan pasangan elektron secara bersama-sama oleh atom-atom yang berikatan. Dengan kata lain, pasangan elektron ini digunakan bersama-sama (shared electrons - elektron sekutu). Sebagai contoh sederhana adalah adanya ikatan kovalen yang terjadi antara unsur hidrogen dengan oksigen membentuk air (H2O). Masing-masing ikatan kovalen mengandung dua elektron, yaitu satu berasal dari hidrogen dan satunya lagi berasal dari oksigen.
Atom berikatan kovalen dengan atom lain untuk mencapai kestabilan. Dengan adanya "penyekutuan" elektron valensi, atom dapat memenuhi orbital atom terluarnya dan mencapai kestabilan.
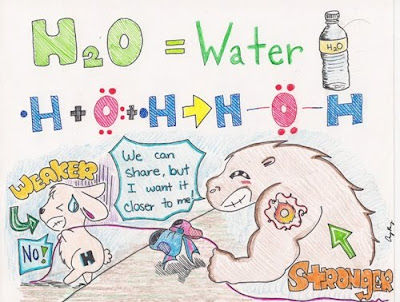
Contoh senyawa kovalen polar adalah air, sulfida, ozon, dsb.
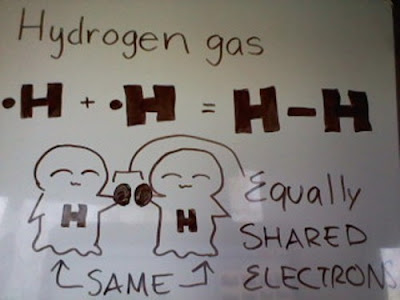
Contoh senyawa kovalen nonpolar adalah gas hidrogen, gas nitrogen, dsb.
Atom berikatan kovalen dengan atom lain untuk mencapai kestabilan. Dengan adanya "penyekutuan" elektron valensi, atom dapat memenuhi orbital atom terluarnya dan mencapai kestabilan.
Ikatan Kovalen Polar dan Non Polar
Ikatan Kovalen Polar
Ikatan kovalen polar adalah ikatan kovalen yang terbentuk ketika elektron sekutu di antara atom tidakbenar-benar dipakai bersama. Hal ini terjadi ketika satu atom mempunyai elektronegativitas yang lebih tinggi daripada atom yang lainnya. Atom yang mempunyai elektronegativitas yang tinggi mempunyai tarikan elektron yang lebih kuat. Akibatnya elektron sekutu akan lebih dekat ke atom yang mempunyai elektronegativitas tinggi. Dengan kata lain, akan menjauhi atom yang mempunyai elektronegativitas rendah. Ikatan kovalen polar menjadikan molekul yang terbentuk mempunyai potensial elektrostatis. Potensial ini akan membuat molekul lebih polar, karena ikatan yang terbentuk dengan molekul polar lain relatif lemah. Ilustrasi ikatan kovalen polar adalah sebagai berikut: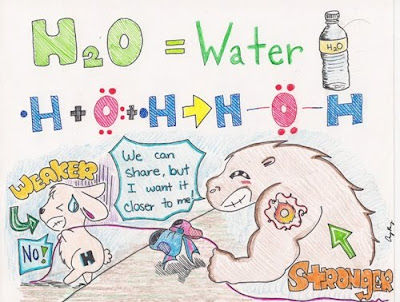
Contoh senyawa kovalen polar adalah air, sulfida, ozon, dsb.
Ikatan Kovalen Non Polar
Ikatan kovalen nonpolar adalah ikatan kovalen yang terbentuk ketika atom membagikan elektronnya secara setara (sama). Biasanya terjadi ketika ada atom mempunyai afinitas elektron yang sama atau hampir sama. Semakin dekat nilai afinitas elektron, maka semakin kuat ikatannya. Ikatan kovalen nonpolar terjadi pada molekul gas, atau yang sering disebut sebagai molekul diatomik. Ikatan kovalen nonpolar mempunyai konsep yang sama dengan ikatan kovalen polar, yaitu atom yang mempunyai nilai elekronegativitas tinggi akan menarik elektron lebih kuat. Pernyataan tesebut benar, namun jika terjadi pada molekul diatom (dimana atom penyusunnya adalah sama) maka elektronegativitas juga sama. Ilustrasi ikatan kovalen nonpolar adalah sebagai berikut:
Contoh senyawa kovalen nonpolar adalah gas hidrogen, gas nitrogen, dsb.
Rating:
100%
based on 10 ratings.
5 user reviews.




0 komentar:
Posting Komentar