Elektrolisis merupakan proses disosiasi suatu elektrolit dengan bantuan arus listrik. Karena dinilai bermanfaat, sekarang banyak dikembangkan teknik elektrolisis untuk keperluan industri. Halaman ini akan menjelaskan penerapan elektrolisis dalam kehidupan manusia. Banyak sekali manfaat elektrolisis, di antaranya adalah:
Membran ini mengijinkan kation terhidrasi untuk melewati kompartemen antara anoda dan katoda, tetapi tidak untuk anion OH- dan Cl-. Dengan demikian proses ini menghasilkan natrium hidroksida tanpa kontaminasi ion klorida.
Pemurnian Logam
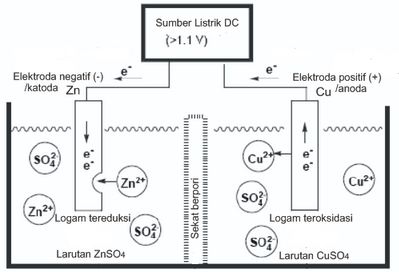
Pada pemurnian logam, anoda yang dipakai adalah logam tak murni (kotor). Pengotor akan terlepas selama proses elektrolisis ketika logam bergerak dari anoda ke katoda. Selama proses ini, katoda mengandung dekomposisi logam murni dari larutan yang berisi ion logam. Sebagai contoh, tembaga dimurnikan melalui elektrolisis yang membutuhkan konduktivitas listrik yang tinggi. Pada proses ini, katoda adalah tembaga murni, sedangkan anoda adalah tembaga kotor. Ion Cu2+ dari anoda bergerak melalui larutan tembaga(II) sulfat menuju katoda dan berubah menjadi padatan tembaga. Selama proses berlangsung, pengotor akan mengendap di dasar tangki. Hasil samping berupa pengotor disebut sebagai lumpur anoda.Elektrosintesis
Elektrosintesis adalah metode yang menggunakan reaksi elektrolisis untuk menghasilkan produk tertentu. Sebagai contoh adalah elektrosintesis MnO2 yang merupakan bahan baku pembuatan baterai alkalin. Larutan untuk elektrosintesis senyawa MnO2 adalah MnSO4 dalam H2SO4. Berperan sebagai anoda adalah grafit, dimana Mn2+ teroksidasi. Sedangkan di katoda, hidrogen tereduksi dari H+ menjadi H2. Reaksinya adalah sebagai berikut:
Mn2+(aq) + 2 H2O(l) → MnO2(s) + 2H+(aq) + H2(g)
Proses Klor-alkali
Elektrolisis air laut dapat menghasilkan klorin dan basa natrium hidroksida. Ada tiga macam metode berbeda dimana dua komponen tersebut dihasilkan, yaitu sel membran, sel diafragma, dan proses sel merkuri.Proses sel membran
Proses ini lebih efisien daripada yang lain karena tidak menggunakan merkuri dan tidak membutuhkan energi yang besar. Mengandung membran penukar kation yang biasanya terbuat dari polimer fluorokarbon.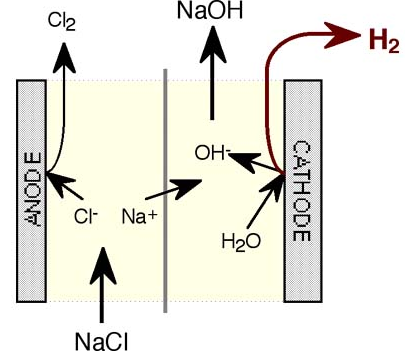 |
| Ilustrasi proses klor-alkali dengan sel membran |